取材是电镜实验的第一步,其操作成功与否直接关系到电镜结果的好坏。为了得到好的结果,请务必按要求做好取材!取材基本要点:快(1min)、准(部位准确)、小(1 mm3)、净(无杂质)、柔(避免机械损伤)。不同的样品,取材细节上有很大区别!
① 快:取材操作要快捷。样品在离体后以最快的速率浸入初固定液,以免长时间缺血缺氧引起组织细胞自溶,并防止微生物繁殖导致样品腐败,破坏精细结构。
② 准:由于电镜标本要求小块取材,为了电镜观察的准确性,取材部位必须要准确,而且,不同实验组的标本尽量取在相同部位(如心肌组织取左心室,则一律取左心室),否则,将无法比较,进而影响观察结果。
③ 小:由于受电镜固定液及包埋剂渗透速度的影响,因此,一般组织块的大小不超过1mm³。
④ 净:尽量少带血液和组织液进入固定液。但切忌用水直接冲洗,可用缓冲液(0.1MPBS)把表面的血液和组织液轻轻冲掉。
⑤ 柔:轻柔的操作可减少人为机械损伤,尽量避免金属器具对组织细胞的夹持、挤压和牵拉,从而影响最后拍摄效果。
注:样品大小跟固定剂有效渗透深度密不可分,固定液有效固定深度为1 mm3,因此要求客户按照此大小送样,样品成功与否80%-90%由前固定取材决定。
1、细胞样品:
① 悬浮细胞:轻微并短暂离心培养液后收集细胞,加入新鲜缓冲液,低温1000rpm/min(离心力不可过大,离心时间不可过长,避免机械挤压导致细胞变形,也可根据具体情况调整)离心5min,弃上清。滴加新鲜缓冲液重悬几分钟,低温1000rpm/min,离心5min,青弃上清,重复2遍。样品加入新鲜的2.5%戊二醛固定液后重悬,4℃固定过夜。收集细胞要肉眼可见细胞沉淀有绿豆大小,弃培养基后加电镜固定液4度避光固定24h(4°渗透速率过慢建议室温0.5h-1h后再放置4°),后续冰袋运输,在保存和运输过程中固定液切勿冷冻结冰。敏感的细胞直接固定,不洗。
② 贴壁细胞:采用轻吹,刮刀(建议采用刮刀法,垂直刮取,避免反复);若用胰酶消化0.5min后立即加入血清终止(贴壁牢的肿瘤细胞,可以消化+刮刀),置于尖底1.5mL离心管中,滴加1小滴固定液立即混匀(勿使液体凝固),低温1000rpm/min离心5-10min,弃上清(不清洗)。收集绿豆大小的细胞沉淀置于尖底1.5mL离心管中。沿管壁小心加满4℃预冷新鲜的2.5%戊二醛固定液(固定液加满离心管,使样品完全浸没在固定液中,建议加完固定液之后重悬下,让样本与固定液充分接触),放置于4°C固定12h后,用泡沫盒加冰袋低温保存运输。
注意:样本管与冰袋隔开,固定液切勿冷冻结冰。 绿豆大小是最佳细胞量,如果样品比较珍贵较难富集也可小米粒大小或半个小米粒大小,样品量过少电镜下可视目标物较少,建议送样前光镜下先确认好细胞状态,细胞培养浓度铺满80%左右,例如用10cm培养皿大多情况能达到送样量。

2、细菌、真菌样本品:
① 液体培养:吸取OD0.5-0.8的培养物,离心后弃培养基,收集菌体沉淀于管底绿豆大小,可以用PBS洗1-2次(此步骤不清洗电镜全是样品碎屑和杂质),弃掉上清液,沿管壁缓慢加入2.5%戊二醛固定液(固定液加满离心管,使样品完全浸没在固定液中),放置于4°C固定12h后,用泡沫盒加冰袋低温保存运输,注意:样本管与冰袋隔开,固定液切勿冷冻结冰。
② 固体培养:从培养基上刮取细胞群落,加入新鲜缓冲液,低温1000rpm/min离心5min后,弃上清。滴加新鲜缓冲液重悬15min,低温1000rpm/min离心5min,弃上清,重复2遍。样品加入戊二醛固定液后重悬,4℃固定过夜。(培养基上样品取材尽可能把琼脂分离,无法分离则需要标注正反面,避免电镜下可视浓度受影响)
注意:含有细胞壁的建议抽真空。
3、组织样本:
a: 浸泡固定:适用于一些能允许在短时间内停止供血而仍保持其功能和结构的器官或组织,以及一些病理检查的样品。其方法是经解剖 (或手术)尽快从机体中取出所需组织,并按取材要求,把组织切成小块,放入离心管内常规固定。
b: 血管灌注固定(对于一些特殊要求的器官:脑、脊髓、睾丸等):适用于取材较复杂或对缺氧较敏感的器官或组织,须采用血管灌注固定。灌注固定一般通过供血的动脉进行,小动物也可经左心室或升主动脉穿刺,行全身灌注。可根据动物的大小选用全身灌注或局部灌注的方式。参考方法:首先用50毫升生理盐水(37℃)清洗血液,接着用50毫升4%多聚甲醛固定液(37℃)快速灌注固定,然后用250-300毫升冷固定液(4℃)慢速灌入,持续5-10钟后精准取材,置组织于戊二醛固定液中,在4℃冰箱中固定。
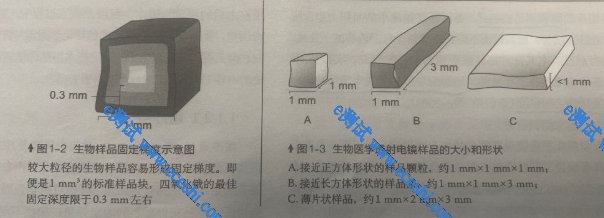
肠、血管、皮肤、肌肉等有方向性样本需切成1mm*3mm*0.5mm长方体小块(如下图B),使用2mL离心管加满2.5%戊二醛固定液,需要提供切面方向,例如横切/纵切,如果不清楚需要提供测试目的,或者效果图,根据测试目的/效果图判断切面;无方向性的组织,如肝脏、肾脏、肺脏等可切成1mm³立方体小块(如下图A),使用2mL离心管加满2.5%戊二醛固定液,放置于4°C固定12h后,用泡沫盒加冰袋低温保存运输。注意:样本管与冰袋隔开,避免固定液结冰。固定液渗透能力有限,超出此范围后组织会无法完全固定,可能会影响后续结果,请务必重视此过程。
特别注意:取材时尽量精确到需要观察的目的部位(如观察肾小球取肾皮质;观察胰岛取胰岛丰富的胰尾;皮肤,肠胃等在固定液中易打卷的组织可将组织粘在滤纸上进行固定)。组织样品需要客户把要观测的区域暴露于表面,避免后续实验室采取半薄定位寻找目标区域,若目标区域较深内部精细结构是无法保留下来的,增加重新送样和复测的风险。
4、植物样本:
取材流程:PBS冲洗样品,确保无泥沙等污染物。然后用锋利刀片或剪刀将样品切成合适大小避免机械拉扯,装入电镜专用2.5%戊二醛+2%PFA多聚甲醛混合固定液中。不需要定位的样品切成1立方毫米大小(如叶片、果实、花粉等),需要定位的样品,切1mm×3mm×0.5mm的长条状(茎、根、表皮等)随后抽气,也可配合离心一起让组织能沉淀到管底,或者塞入棉花。并且提供切面方向,例如横切/纵切。最后样本充分固定后,用泡沫盒加冰袋低温保存运输,注意:样本管与冰袋隔开,固定液切勿冷冻结冰。
















 论文致谢
论文致谢

 预约须知
预约须知
 项目介绍
项目介绍


 结果展示
结果展示



 常见问题
常见问题















